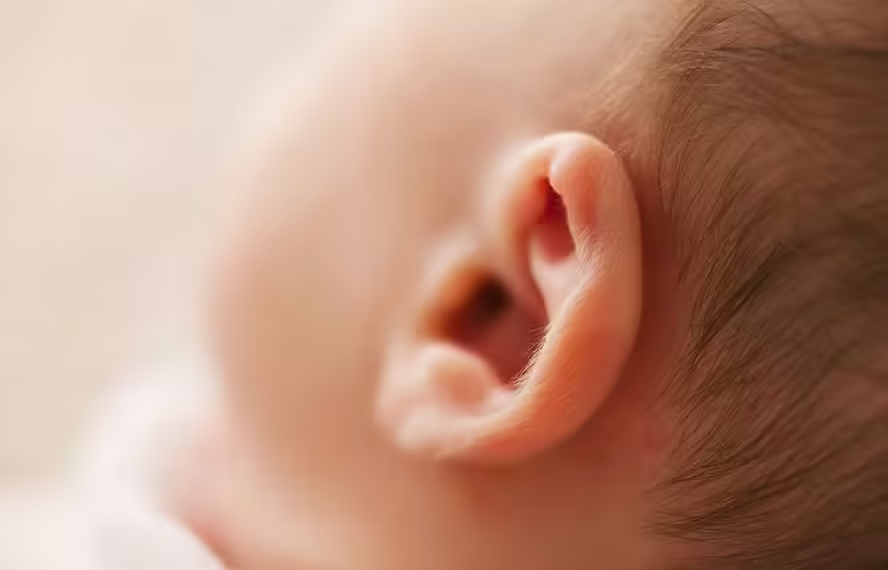
Na China, uma equipe de pesquisadores conseguiu reverter o quadro de surdez hereditária de cinco crianças que, além de desenvolverem suas funções auditivas, também adquiriram melhor percepção da fala e capacidade de determinar a posição dos sons. O estudo é o primeiro ensaio clínico do mundo a administrar uma terapia gênica em ambos os ouvidos e seus resultados foram publicados nesta quarta-feira (5) na revista Nature Medicine.
Estima-se que mais de 430 milhões de pessoas pelo globo são afetadas por perda auditiva incapacitante, dessas, 26 milhões são diagnosticadas com surdez congênita. Segundo a pesquisa, até 60% dos quadros de surdez infantil são causados por fatores genéticos, como a DFNB9, uma mutação no gene OTOF que impede a produção da proteína otoferlina, responsável pela audição funcional.
O estudo investiga exatamente o tratamento dos casos de DFNB9. O objetivo era tratar as crianças de forma que elas alcançassem a capacidade de ouvir sons em três dimensões – algo importante para a comunicação e a realização de tarefas diárias comuns.
“Restaurar a audição em ambos os ouvidos de crianças que nasceram surdas pode maximizar os benefícios da recuperação auditiva”, explica o principal autor do estudo, Yilai Shu, em nota à imprensa. Dessa forma, foram injetadas cópias ativas do transgene OTOF humano transportado pelo vírus adeno-associado (AAV) nos ouvidos internos dos pacientes por meio de uma cirurgia especializada e minimamente invasiva.
Em observação durante um período de 13 a 26 semanas no Eye & ENT Hospital da Universidade Fudan, em Xangai, foram verificados 36 eventos adversos nos pacientes, mas não ocorreu toxicidade limitante da dose ou ferimentos graves. Todas as cinco crianças apresentaram recuperação auditiva em ambos os ouvidos.
“Os resultados são surpreendentes”, afirma Zheng-Yi Chen, coautor sênior do estudo. “Ao longo do processo, vimos a capacidade auditiva das crianças tratadas progredir dramaticamente, além de o tratamento trazer benefícios adicionais, como a capacidade de localização de fonte sonora e melhorias no reconhecimento de fala em ambientes ruidosos.”
Em 2022, a mesma equipe de investigação desenvolveu uma outra terapia gênica para DFNB9 mas, na ocasião, o tratamento era conduzido em apenas um ouvido. Os resultados desses testes foram publicados no The Lancet em janeiro deste ano, revelando o sucesso de melhorias na audição e na fala em cinco das seis crianças acompanhadas.
Shu inicialmente apresentou os dados no 30º Congresso Anual da Sociedade Europeia de Terapia Genética e Celular (ESGCT), em outubro de 2023, tornando-se o primeiro pesquisador no mundo a relatar dados clínicos sobre o uso de terapia gênica para restaurar a audição.
“Os novos resultados confirmam a eficácia do tratamento que relatamos anteriormente. Isso representa um grande e importante passo na terapia gênica para perda auditiva genética”, indica Shu. Atualmente, não existem medicamentos disponíveis para tratar a surdez hereditária.
Chen acrescenta que o seu desejo é que o estudo possa se expandir de forma que a abordagem também possa ser analisada para outros casos de surdez: “Nosso objetivo final é ajudar as pessoas a recuperar a audição, independentemente da causa – seja por outros genes que não o DFNB9 ou até por causas não genéticas”.
Futuro da pesquisa
A investigação continua em andamento e os participantes continuam sendo monitorados. Os autores destacam que ainda são necessários mais trabalhos para estudar e refinar a proposta terapêutica.
Atualmente, o Instituto de Terapia Genética e Celular do Mass General Brigham está ajudando a equipe a traduzir as descobertas científicas. Os pesquisadores também trabalham para desenvolver plataformas e vetores com padrões de boas práticas de fabricação, o que permitiria à equipe testar mais facilmente a abordagem com outros genes no futuro.
Outras preocupações ainda estão sendo consideradas. Por exemplo, entende-se que o estudo bilateral requer mais considerações em comparação com o estudo unilateral, uma vez que as operações em ambas as orelhas, no decurso de uma cirurgia, duplicam o tempo cirúrgico. Além disso, ao injetar doses duplas de AAV no corpo, é provável que a resposta imunitária seja mais forte e o potencial para efeitos adversos possa ser maior.
Olhando para o futuro, os especialistas apontam para a necessidade de conduzir mais testes com pacientes, bem como traçar um acompanhamento mais longo, mantendo a análise contínua das terapias gênicas e dos implantes cocleares em ensaios randomizados maiores será valiosa.
Fonte: Revista Galileu