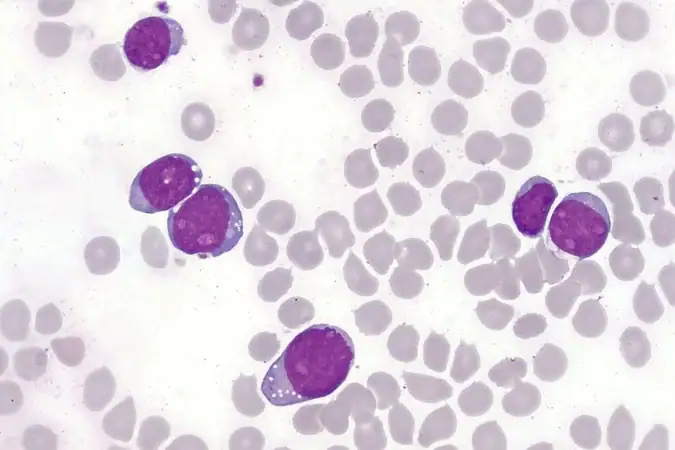
Uma nova terapia que usa células imunológicas geneticamente modificadas levou à remissão pacientes de um tipo raro e agressivo de câncer no sangue, a leucemia linfoblástica aguda de células T (LLA-T). O tratamento foi desenvolvido por pesquisadores da Universidade College London (UCL), no Reino Unido, e do Hospital Great Ormond Street (Gosh). As 11 pessoas que participaram do estudo, incluindo crianças e adultos, já haviam se submetido a outras abordagens terapêuticas, sem sucesso.
A chamada terapia gênica pioneira mundial (BE-CAR7) utiliza células imunológicas modificadas para abordar a LLA-T, antes considerada intratável. A edição de bases é uma versão avançada da tecnologia CRISPR, que permite alterar com precisão letras individuais do código de DNA dentro de tecidos vivos. Segundo os pesquisadores, que relataram o tratamento na revista New England Journal of Medicine, a expectativa é “ajudar os pacientes a alcançarem a remissão, oferecendo uma nova esperança para famílias que enfrentam esse câncer agressivo”.
Em 2022, pesquisadores do Gosh e da UCL administraram o primeiro tratamento do mundo feito com a tecnologia de edição de bases a Alyssa, uma menina de 13 anos da cidade inglesa de Leicester. Agora, outras oito crianças e dois adultos receberam a terapia. Desses, 82% alcançaram remissões significativas que permitiram a eles prosseguir para o transplante de células-tronco, já livres da doença.
Além disso, 64% dos pacientes continuam em remissão, sendo que os primeiros a receberem o tratamento, há três anos, não têm qualquer sinal do câncer e levam uma vida normal, sem se submeter a outras terapias. Os efeitos colaterais esperados, incluindo baixa contagem sanguínea, síndrome de liberação de citocinas e erupções cutâneas, foram toleráveis, disseram os autores.
Precisão
“Anteriormente, mostramos resultados promissores com a edição genômica de precisão em crianças com câncer sanguíneo agressivo, e esse número maior de pacientes confirma o impacto desse tipo de tratamento”, disse, em nota, Waseem Qasim, que liderou a pesquisa e é professor de terapia celular e gênica na UCL. “Mostramos que células CAR-T universais ou ‘prontas para uso’, podem buscar e destruir casos muito resistentes de leucemia CD7 .”
Embora a maioria das crianças com leucemia de células T responda bem aos tratamentos padrão, cerca de 20% podem não se beneficiar. “São esses pacientes que precisam desesperadamente de melhores opções, e essa pesquisa oferece esperança de um prognóstico melhor”, escreveram os autores do estudo.
O oncologista Márcio Almeida, membro da Sociedade Brasileira de Oncologia Clínica (SBOC), explica que a terapia descrita tem várias diferenças em relação à quimioterapia e ao transplante tradicional. “Ao contrário da quimioterapia, que ataca indiscriminadamente células em divisão (saudáveis e cancerosas), a BE-CAR7 mira especificamente células T cancerosas por meio de marcadores reconhecíveis, o que pode reduzir danos colaterais ao restante do corpo”, diz.
Velocidade
Além disso, o médico destaca a velocidade e profundidade da remissão e a redução de riscos genéticos. “A edição por base-editing evita cortes no DNA e, consequentemente, pode reduzir o risco de danificar o genoma das células, algo que é preocupação em estratégias mais invasivas de modificação genética”, observa. “Essa abordagem representa uma forma de imunoterapia de precisão mais seletiva, com maior potência e potencialmente menos tóxica do que tratamentos convencionais.”
Bob Phillips, consultor em oncologia pediátrica na Universidade de York, no Reino Unido, destaca, porém, que o tratamento com células CAR-T universais não é “uma bala de prata para todas as doenças de célula T recidivantes”. “Não se trata de uma terapia simples, de primeira linha para leucemia. Porém, essa é uma abordagem importante que nos permite uma linha extra de tratamento para alguns pacientes em situações altamente específicas”, diz Philips, que não participou do estudo.
Manipulação sem cortes
A imunoterapia com células CAR-T tornou-se recentemente disponível para tratar vários tipos de câncer no sangue. A abordagem usa células imunológicas, chamadas T, e as modifica para que exibam proteínas específicas em sua superfície, chamadas receptores de antígenos quiméricos (CARs). Os CARs podem reconhecer e atacar marcadores das células cancerígenas, que são destruídas em seguida.
Na pesquisa britânica, os pesquisadores usaram a edição de bases para produzir as células BE- -CAR7, evitando o corte do DNA e reduzindo o risco de danos cromossômicos. Conforme relatado em 2022, as complexas alterações genéticas geraram bancos armazenáveis de células CAR-T “universais”, capazes de encontrar e atacar a leucemia de células T quando administradas a pacientes.
As células CAR-T “universais” do estudo foram produzidas a partir de glóbulos brancos de doadores saudáveis.
Três perguntas para Márcio Almeida, oncologista e membro da Sociedade Brasileira de Oncologia Clínica (SBOC):
O que caracteriza a nova terapia?
A terapia, chamada BE-CAR7, consiste em infundir no paciente células T saudáveis de doadores, já editadas geneticamente por uma técnica conhecida como base-editing, uma versão avançada de edição genômica que altera “letras” do DNA sem fazer cortes no genoma. Essas células são equipadas com um receptor especial (CAR) que permite reconhecer e destruir células de leucemia. Após a infusão, as células editadas eliminam rapidamente as células T do corpo, tanto as saudáveis quanto as cancerosas. Se a leucemia for erradicada dentro de cerca de quatro semanas, o paciente segue para um transplante de medula óssea para reconstruir o sistema imunológico saudável.
A abordagem usa células de doadores, e não do próprio paciente. Isso pode facilitar o acesso ao tratamento no futuro?
As células usadas não vêm do próprio paciente (como na maioria das terapias tradicionais ou das primeiras gerações de terapias CAR-T), mas de doadores saudáveis, editadas e “armazenadas” previamente. Isso cria um estoque de células “universais” prontas para uso (“off-the-shelf”). Esse formato pode facilitar o acesso no futuro, porque não dependerá da coleta de células do paciente, que nem sempre é possível (por baixa contagem, exaustão dos linfócitos, fragilidade etc.). O tratamento poderá ser administrado rapidamente, sem o tempo de produção individualizada, importante em leucemias agressivas, em que a velocidade faz diferença e ainda pode reduzir custos e complexidade logística, favorecendo maior disponibilidade caso aprovado para uso amplo.
É possível estimar quando o tratamento estará disponível?
Apesar dos resultados animadores, ainda é cedo para afirmar com precisão quando a BE-CAR7 estará disponível de modo generalizado. Alguns fatores como, por exemplo, o estudo até agora envolveu apenas 11 pacientes (nove crianças e dois adultos).
Manipulação sem cortes
A imunoterapia com células CAR-T tornou-se recentemente disponível para tratar vários tipos de câncer no sangue. A abordagem usa células imunológicas, chamadas T, e as modifica para que exibam proteínas específicas em sua superfície, chamadas receptores de antígenos quiméricos (CARs). Os CARs podem reconhecer e atacar marcadores das células cancerígenas, que são destruídas em seguida.
Na pesquisa britânica, os pesquisadores usaram a edição de bases para produzir as células BE-CAR7, evitando o corte do DNA e reduzindo o risco de danos cromossômicos. Conforme relatado em 2022, as complexas alterações genéticas geraram bancos armazenáveis de células CAR-T “universais”, capazes de encontrar e atacar a leucemia de células T quando administradas a pacientes.
As células CAR-T “universais” do estudo foram produzidas a partir de glóbulos brancos de doadores saudáveis.
Fonte: Universidade
College London
Por Correio Braziliense